Пенициллин (история изобретения). Александр Флеминг - история создания пенициллина
Известно, что еще в XV-XVI вв. в народной медицине для лечения гноящихся ран использовалась зеленая плесень. Ею, например, умела лечить Алена Арзамасская, сподвижница Степана Разина, русская Жанна д"Арк. Попытки накладывать плесень непосредственно на раневую поверхность давали, как это ни странно, хорошие результаты.
Не следует считать пенициллин единственной заслугой А. Флеминга; еще в 1922 г. он совершил свое первое важное открытие - выделил из человеческих тканей вещество, обладающее способностью довольно активно растворять некоторые виды микробов. Открытие это было сделано почти случайно при попытке выделить бактерии - возбудители обычной простуды. Профессор А. Райт, под чьим руководством А. Флеминг продолжал свою исследовательскую работу, назвал новое вещество лизоцимом (лизис - разрушение микроорганизмов). Правда, оказалось, что лизоцим малоэффективен в борьбе с наиболее опасными болезнетворными микробами, хотя успешно уничтожает относительно менее опасные микроорганизмы.
Таким образом, применение лизоцима в медицинской практике имело не очень широкие перспективы. Это подтолкнуло А. Флеминга к дальнейшему поиску эффективных и при этом по возможности безвредных для человека антибактериальных препаратов. Надо сказать, что еще в 1908 г. он проводил эксперименты с препаратом под названием «сальварсан», который лаборатория профессора А. Райта получила для всесторонних исследований в числе первых в Европе. Препарат этот был создан талантливым немецким ученым П. Эрлихом (Нобелевская премия совместно с И. И. Мечниковым, 1908 г.). Тот искал препарат, убийственный для болезнетворных микроорганизмов, но безопасный для пациента, так называемую магическую пулю. Сальварсан был довольно эффективным противо-сифилитическим средством, но оказывал на организм побочное действие токсического характера. Это были лишь первые маленькие шаги в сторону создания современных противомикробных и химиотерапевтических препаратов.
Базируясь на учении об антибиозе (подавлении одних микроорганизмов другими), основы которого были заложены Л. Пастером и нашим великим соотечественником И. И. Мечниковым, А. Флеминг в 1929 г. установил, что лечебное действие зеленой плесени обусловлено особым веществом, выделяемым ею в окружающую среду.
Все гениальное открывается случайно?
Первое упоминание об антибактериальной терапии?
Интересно, что в Библии мы встречаем невероятно точное указание на свойства полукустарниковом растения - иссоп. Вот фрагмент Псалма 50, который, кстати, вспомнил и А. Флеминг: «Окропи меня иссопом, и буду чист; омой меня, и буду белее снега».
Попытаемся воссоздать цепь почти невероятных случайностей и совпадений, предшествовавших великому открытию. Первопричиной стала, как ни странно, неряшливость А. Флеминга. Рассеянность свойственна многим ученым, но далеко не всегда она приводит к таким позитивным результатам. Итак, А. Флеминг не очищал чашки из-под исследуемых культур по нескольку недель, в итоге его рабочее место оказывалось заваленным полусотней чашек. Правда, в процессе уборки он скрупулезно исследовал каждую чашку из опасения пропустить что-либо важное. И не пропустил.
В один прекрасный день он обнаружил в одной из чашек пушистую плесень, которая подавляла рост посеянной в этой чашке культуры стафилококков. Выглядело это так: цепочки стафилококков вокруг плесени исчезли, и на месте желтой мутной массы виднелись капли, напоминавшие росу. Убрав плесень, А. Флеминг увидел, что «бульон, на котором разрослась плесень, приобрел отчетливо выраженную способность подавлять рост микроорганизмов, а также бактерицидные и бактериологические свойства по отношению ко многим распространенным патогенным бактериям».
По всей видимости, споры плесени были занесены через окно из лаборатории, где культивировались образцы плесени, взятые из домов пациентов, страдающих бронхиальной астмой, для получения десенсибилизирующих экстрактов. Ученый оставил чашку на столе и уехал на отдых. Лондонская погода сыграла свою роль: похолодание благоприятствовало росту плесени, а последовавшее потепление - росту бактерий. Если бы из цепочки случайных совпадений выпало хотя бы одно событие, кто знает, когда бы человечество узнало про пенициллин. Плесень, которой была заражена культура стафилококков, относилась к довольно редкому виду рода Penicillium - P. Notatum , который был впервые найден на сгнившем иссопе (полукустарниковом растении, содержащем эфирное масло и использующемся в качестве пряности);
Достоинства нового изобретения
В ходе дальнейших исследований выяснилось, что, к счастью, даже в больших дозах пенициллин нетоксичен для подопытных животных и способен убивать весьма устойчивые болезнетворные микроорганизмы. В больнице Св. Марии не было биохимиков, в результате чего не удалось выделить пенициллин в пригодном для инъекций виде. Эту работу провели в Оксфорде X. У. флори и Э. Б. Чейн лишь в 1938 г. Пенициллин канул бы в небытие, если бы ранее не произошло открытие А. Флемингом лизоцима (вот тут-то он действительно пригодился!). Именно это открытие подвигло оксфордских ученых заняться изучением лечебных свойств пенициллина, в результате чего препарат был выделен в чистом виде в форме бензилпенициллина и испытан клинически. Уже самые первые исследования А. Флеминга дали целый ряд бесценных сведений о пенициллине. Он писал, что это «эффективная антибактериальная субстанция, оказывающая выраженное действие на пиогенные (т. е. вызывающие образование гноя) кокки и палочки дифтерийной группы. Пенициллин даже в огромных дозах не токсичен для животных. Можно предположить, что он окажется эффективным антисептиком при наружной обработке участков, пораженных чувствительными к пенициллину микробами, или при его введении внутрь».
Лекарство получено, но как его применять?
Аналогично Пастеровскому институту в Париже, отделение вакцинации в больнице Св. Марии» где работал А. Флеминг, существовало и получало финансирование на исследования благодаря продаже вакцин. Ученый обнаружил, что в процессе приготовления вакцин пенициллин защищает культуры от стафилококка. Это было небольшое, но серьезное достижение, и А. Флеминг широко пользовался им, еженедельно отдавая указание изготовить большие партии бульона на основе пеницилла. Он делился образцами культуры Penicillium с коллегами в других лабораториях, но, как ни странно, А. Флеминг не сделал столь очевидного шага, который 12 лет спустя был предпринят X. У. Флори и состоял в том, чтобы установить, будут ли спасены подопытные мыши от смертельной инфекции, если лечить их инъекциями пенициллинового бульона. Забегая вперед, скажем, что этим мышам исключительно повезло. А. Флеминг лишь назначил бульон нескольким пациентам для наружного применения. Однако результаты были весьма и весьма противоречивыми. Раствор не только с трудом поддавался очистке в значительном объеме, но и оказывался нестабильным. Кроме того, А. Флеминг ни разу не упомянул о пенициллине ни в одной из 27 статей или лекций, опубликованных им в 1930-1940 гг., даже когда речь в них шла о веществах, вызывающих гибель бактерий. Впрочем, это не помешало ученому получить все причитающиеся ему почести и Нобелевскую премию по физиологии и медицине в 1945 г. Понадобилось длительное время, прежде чем ученые сделали заключение о безопасности пенициллина, как для человека, так и для животного.
Кто же все-таки первым изобрел пенициллин?
А что в это время происходило в лабораториях нашей страны? Неужели отечественные ученые сидели, сложа руки? Конечно, это не так. Многие читали трилогию В. А. Каверина «Открытая книга», однако далеко не все знают, что у главной героини, доктора Татьяны Власенковой, был прототип - Зинаида Виссарионовна Ермольева (1898-1974), выдающийся ученый-микробиолог, создатель целого ряда отечественных антибиотиков. Кроме того, 3. В. Ермольева первой из отечественных ученых начала изучать интерферон как противовирусное средство. Действительный член АМН, она внесла огромный вклад в российскую науку. На выбор профессии 3. В. Ермольевой повлияла история смерти ее любимого композитора. Известно, что П. И. Чайковский скончался, заразившись холерой. По окончании университета 3. В. Ермольева была оставлена ассистентом на кафедре микробиологии; одновременно она заведовала бактериологическим отделением Северо-Кавказского бактериологического института. Когда в 1922 г. В Ростове-на-Дону вспыхнула эпидемия холеры, она, игнорируя смертельную опасность, изучала это заболевание, что называется, на месте. Позже она провела опаснейший эксперимент с самозаражением, результатом которого стало значительное научное открытие.
В годы Великой Отечественной войны, наблюдая за ранеными, 3. В. Ермольева видела, что многие из них умирают не непосредственно от ран, а от заражения крови. К тому времени исследования ее лаборатории абсолютно независимо от англичан показали, что некоторые плесени задерживают рост бактерий. 3. В. Ермольева, разумеется, знала, что в 1929 г. А. Флеминг получил из плесени пенициллин, но выделить его в чистом виде так и не смог, т. к. препарат оказался весьма нестойким. Знала она и о том, что уже давно наши соотечественники еще на уровне народной медицины, знахарства заметили лечебные свойства плесени. Но при этом в отличие от А. Флеминга 3. В. Ермольеву судьба не баловала счастливыми случайностями. В 1943 г. У. X. Флори и Э. Чейн смогли наладить выпуск пенициллина в промышленных масштабах, однако для этого им пришлось организовывать производство в США. 3. В. Ермольева, на тот момент стоявшая во главе Всесоюзного института экспериментальной медицины, поставила перед собой цель получить пенициллин исключительно из отечественного сырья. Надо отдать должное ее упорству - в 1942 г. первые порции советского пенициллина были получены. Величайшей и неоспоримой заслугой 3. В. Ермольевой явилось то, что она не только получила пенициллин, но и сумела наладить массовое производство первого отечественного антибиотика. При этом следует учесть, что шла Великая Отечественная война, остро ощущалась нехватка самых простых и нужных вещей. В то же время потребность в пенициллине росла. И 3. В. Ермольева сделала невозможное: она сумела обеспечить не только количество, но и качество, вернее, силу препарата.
Сколько раненых обязаны ей жизнью, не поддается даже примерному подсчету. Создание советского пенициллина стало своеобразным толчком для создания целого ряда других антибиотиков: первых отечественных образцов стрептомицина, тетрациклина, левомицетина и экмолина - первого антибиотика животного происхождения, выделенного из молок осетровых рыб. Относительно недавно появилось сообщение, за достоверность которого пока сложно ручаться. Вот оно: пенициллин был обнаружен еще до А. Флеминга неким студентом-медиком Эрнестом Августином Дюшенсне, который в своей диссертационной работе подробно описал открытый им удивительно эффективный препарат для борьбы с различными бактериями, пагубно влияющими на человеческий организм. Свое научное открытие Э. Дюшенсне закончить не получилось из-за скоротечной болезни, повлекшей за собой смерть. Однако А. Флеминг и понятия не имел об открытии молодого исследователя. И только совсем недавно в Леоне (Франция) была случайно найдена диссерта ция Э. Дюшенсне.
Кстати, патент на изобретение пенициллина не выдан никому. А. Флеминг, Э. Чейн и У. X. Флори, получившие за его открытие одну Нобелевскую премию на троих, наотрез отказались получать патенты. Они сочли, что вещество, обладающее всеми шансами спасти все человечество, не должно быть источником наживы, золотой жилой. Этот научный прорыв единственный таких масштабов, на который никто и никогда не предъявлял авторских прав.
Стоит упомянуть, что, победив многие распространенные и опасные инфекционные болезни, пенициллин продлил человеческую жизнь в среднем на 30-35 лет!
Начало эры антибиотиков
Итак, в медицине началась новая эра - эра антибиотиков. «Подобное лечится подобным» - этот принцип известен врачам с древнейших времен. Так почему бы не бороться с одними микроорганизмами при помощи других? Эффект превзошел самые смелые ожидания; кроме того, открытие пенициллина положило начало поиску новых антибиотиков и источников их получения. Пенициллинам на момент открытия были свойственны высокая химиотерапевтическая активность и широкий спектр действия, что приближало их к идеальным препаратам. Действие пенициллинов направлено на определенные «мишени» в клетках микроорганизмов, отсутствующие у животных клеток.
Справка. Пенициллины относятся к обширному классу гамма-лактамных антибиотиков. Сюда же относятся цефалоспорины, карбапенемы и монобактамы. Общим в структуре этих антибиотиков является наличие ß -лактамного кольца, ß - лактамные антибиотики составляют основу современной химиотерапии бактериальных инфекций.
Антибиотики нападают - бактерии защищаются, бактерии нападают антибиотики защищаются
Пенициллины обладают бактерицидным свойством, т. е. губительно воздействуют на бактерии. Главный объект воздействия - это пенициллино-связывающие белки бактерий, которые являются ферментами заключительного этапа синтеза клеточной стенки бактерий. Блокирование антибиотиком синтеза пептидогликана приводит к нарушению синтеза клеточной стенки и в конечном счете к гибели бактерии. В процессе эволюции микробы научились защищаться. Они выделяют специальное вещество, разрушающее антибиотик. Это тоже фермент, носящий устрашающее название ß -лактамазы, которая разрушает ß -лактамное кольцо антибиотика. Но наука не стоит на месте, появились новые антибиотики, содержащие так называемые ингибиторы (ß -лактамаз - клавулановая кислота, клавуланат, сульбактам и тазобактам). Такие антибиотики называют пенициллиназо-защищенным и.
Общие особенности антибактериальных препаратов
Антибиотики - это вещества, избирательно подавляющие жизнедеятельность микроорганизмов. Под «избирательным влиянием» подразумевается активность исключительно во взаимоотношении микроорганизмов при сохранении жизнеспособности клеток хозяина и воздействие не на все, а лишь на определенные роды и виды микроорганизмов. Например, фузидиевая кислота имеет высокую активность в отношении стафилококков, включая метициллино-резистентные, но не действует на пневмококки БГСА. С избирательностью близко связано представление об обширности спектра активности антибактериальных препаратов. Тем не менее, с позиций сегодняшнего дня разделение антибиотиков на препараты широкого и узкого спектра действия представляется условным и подвергается серьезной критике по большей части из-за отсутствия критериев для такого деления. Неправильным является суждение о том, что лекарственные средства широкого круга действия являются более надежными, эффективными.
Путь, ведущий в никуда
Господа, последнее слово будет за микробами!
Луи Пастер
Всем микроскопическим врагам человеческого рода объявлена война не на жизнь, а на смерть. Ведется она пока с переменным успехом, однако некоторые болезни уже отступили, похоже, навсегда, например натуральная оспа. Но при этом остается оспа верблюдов, коров, а также оспа обезьян. Однако и с оспой не все так просто. С середины 1980-х гг. случаи заболевания натуральной оспой не регистрируются. В связи с этим уже довольно давно дети не прививаются от оспы. Таким образом, в человеческой популяции с каждым годом уменьшается число людей, устойчивых к вирусу натуральной оспы. А вирус этот никуда не делся. Он может сохраняться на костях погибших от оспы людей (далеко не все трупы были сожжены, некоторые и жечь-то было некому) сколь угодно долго. И когда-нибудь обязательно произойдет встреча непривитого человека, например археолога, с вирусом. Л. Пастер был прав. На второй план отошли многие ранее смертельные заболевания - дизентерия, холера, гнойные инфекции, воспаление легких и др. Однако сап, которого не наблюдалось почти 100 лет, похоже, вернулся. В ряде стран наблюдаются вспышки полиомиелита спустя десятилетия, прошедшие без этого грозного заболевания. Добавились новые угрозы, в частности птичий грипп. От вируса птичьего гриппа уже погибают хищные млекопитающие. Открытые границы сделали невозможной борьбу с микробами в отдельно взятом государстве. Если ранее существовали заболевания, более свойственные какому-либо региону, то в настоящий момент размываются даже границы климатических зон, более характерных для конкретного вида патологии. Разумеется, специфические инфекции тропической зоны пока не грозят жителям Крайнего Севера, но, например, половые инфекции, СПИД, гепатиты В, С в результате процесса всеобщей глобализации превратились в действительно глобальную угрозу. Малярия распространилась от жарких стран вплоть до полярного круга.
Причиной возникновения классических инфекционных болезней являются патогенные микроорганизмы, представленные бактериями (такими, как бациллы, кокки, спирохеты» риккетсии), вирусами ряда семейств (герпесвирусами, аденовирусами, паповавирусами, парвовирусами, ортомиксовирусами, парамиксовирусами, ретровирусами, буньявирусами, тогавирусами, коронавирусами, пикорнавирусами, ареновирусами и рабдовирусами), грибами (оомицетами, аскомицетами, актиномицетами, базидиомицетами, дейтеромицетами) и простейшими (жгутиковыми, саркодовыми, споровиками, ресничными). Кроме патогенных микроорганизмов, существует большая группа условно-патогенных микробов, способных провоцировать развитие так называемых оппортунистических инфекций - патологического процесса у людей с различными иммунодефицитами. Поскольку была наглядно доказана возможность получения антибиотических препаратов из микроорганизмов, открытие новых препаратов стало вопросом времени. Обычно получается так, что время работает не на врачей и микробиологов, а, напротив, на представителей болезнетворной микрофлоры. Однако поначалу появился даже повод для оптимизма.
Хронология появления антибиотиков
В 1939 г. был выделен грамицидин» затем в хронологическом порядке - стрептомицин (в 1942 г.), хлортстрациклин (в 1945 г.), левомицетин (в 1947 г.), а к 1950 г. было описано уже более 100 антибиотиков. Необходимо отметить, что в 1950-1960 гг. это вызвало преждевременную эйфорию в медицинских кругах. В 1969 г. Конгрессу США был представлен весьма оптимистичный доклад, содержавший такие смелые утверждения, как «книга инфекционных заболеваний будет закрыта ».
Одной из наиболее масштабных ошибок человечества является попытка обогнать естественный эволюционный процесс» ведь человек лишь часть этого процесса. Поиск новых антибиотиков - процесс весьма долгий, кропотливый, требующий серьезного финансирования. Многие антибиотики были выделены из микроорганизмов, средой обитания которых является почва. Выяснилось, что в почве живут смертельные враги ряда патогенных для человека микроорганизмов - возбудителей тифа, холеры, дизентерии, туберкулеза и др. Стрептомицин, использующийся для лечения туберкулеза до настоящего времени, тоже был выделен из почвенных микроорганизмов. Для того чтобы отобрать нужный штамм, 3. Ваксман (первооткрыватель стрептомицина) изучил в течение 3 лет свыше 500 культур, прежде чем обнаружил подходящую - ту, которая выделяет в среду обитания больше стрептомицина, чем другие культуры. В ходе научных изысканий тщательно изучаются и отбраковываются многие тысячи культур микроорганизмов. И лишь единичные экземпляры используются для последующего изучения. Однако это не означает, что все они потом станут источником для получения новых лекарственных препаратов. Чрезвычайно низкая продуктивность культур, техническая сложность выделения и последующей очистки лекарственных веществ ставят дополнительные зачастую непреодолимые барьеры на пути новых препаратов. А новые антибиотики необходимы, как воздух. Кто мог предполагать, что жизнеспособность микробов станет такой серьезной проблемой? К тому же выявлялись все новые возбудители инфекционных болезней» и спектр активности уже имеющихся препаратов становился недостаточным для эффективной борьбы с ними. Микроорганизмы очень быстро адаптировались и становились невосприимчивыми к действию, казалось бы, уже проверенных препаратов. Предвидеть возникновение лекарственной устойчивости микробов было вполне реально, и совершенно необязательно быть для этого талантливым фантастом. Скорее, роль гениальных провидцев должны были сыграть скептики из научных кругов. Но если кто-то и предрекал что-то подобное, то его голос не был услышан, его мнение не было принято к сведению. А ведь похожая ситуация уже наблюдалась при внедрении инсектицида ДДТ в 1940-е гг. Сначала мухи, против которых и была предпринята столь массированная атака, практически полностью исчезли, но затем расплодились в огромном количестве, причем новое поколение мух было к ДДТ устойчиво, что говорит о генетическом закреплении этого признака. Что же касается микроорганизмов, то еще А. Флеминг обнаружил, что последующие поколения стафилококков образовывали клеточные стенки со структурой, устойчивой к воздействию пенициллина. О положении дел, которое может сложиться при таком векторе развития событий, предупреждал более 30 лет назад академик С. Шварц. Он говорил: «Что бы ни случилось на верхних этажах природы, какие бы катаклизмы ни потрясли биосферу... высшая эффективность использования энергии на уровне клеток и тканей гарантирует жизнь организмам, которые и восстановят жизнь на всех ее этажах в той форме, которая соответствует новым условиям среды». Некоторые бактерии могут отторгать антибиотики по мере их вторжения внутрь или нейтрализовывать их. По этой причине параллельно с поиском новых видов природных антибиотиков велись углубленные работы по анализу структуры уже известных веществ, чтобы затем, базируясь на этих данных, модифицировать их, создавая новые, значительно более эффективные и безопасные препараты. Новым этапом эволюции антибиотиков, несомненно, стало изобретение и внедрение в медицинскую практику полусинтетических препаратов, сходных по строению или по типу воздействия с природными антибиотиками. В 1957 г. впервые удалось выделить феноксиметилпенициллин, устойчивый к действию соляной кислоты желудочного сока, который можно принимать в таблетированной форме. Пенициллины природного происхождения были совершенно неэффективны при приеме внутрь, так как в кислой среде желудка теряли свою активность. Позже был придуман метод производства полусинтетических пенициллинов. С этой целью молекулу пенициллина «разрезали» посредством воздействия фермента пенициллиназы и, применяя одну из частей, синтезировали новые соединения. С помощью этой методики удалось создать препараты значительно более широкого спектра антимикробного действия (амоксициллин, ампициллин, карбенициллин), чем исходный пенициллин. Не менее известный антибиотик, цефалоспорин, впервые выделенный в 1945 г. из сточных вод на острове Сардиния, стал родоначальником новой группы полусинтетических антибиотиков - цефалоспоринов, оказывающих мощное антибактериальное действие и почти безвредных для человека. Различных цефалоспоринов уже больше 100. Некоторые из них могут уничтожать как грамположительные, так и грамотрицательные микроорганизмы, другие действуют на устойчивые штаммы бактерий. Понятно, что любой антибиотик оказывает свое определенное избирательное действие на строго определенные виды микроорганизмов. По причине такого избирательного действия значительная часть антибиотиков способна сводить на нет многие виды патогенных микроорганизмов, действуя в безвредных или почти безвредных для организма концентрациях. Именно такой тип антибиотических препаратов чрезвычайно часто и широко применяют для лечения разнообразных инфекционных заболеваний. Главными источниками, которые используют для получения антибиотиков, являются микроорганизмы со средой обитания в почве и воде, где они непрерывно взаимодействуют, вступая между собой в разнообразные взаимоотношения, которые могут являться нейтральными, антагонистичными или взаимовыгодными. Ярким примером могут служить гнилостные бактерии, которые создают хорошие условия для нормальной жизнедеятельности нитрифицирующих бактерий. Однако зачастую взаимоотношения микроорганизмов бывают антагонистическими, т. е. направленными друг против друга. Это вполне понятно, поскольку лишь подобным путем в природе могло изначально поддерживаться экологическое равновесие огромного количества биологических форм. Российский ученый И. И. Мечников, намного опережая свое время, первым предложил применять на практике антагонизм между бактериями. Он советовал подавлять жизнедеятельность гнилостных бактерий, которые постоянно обитают в кишечнике человека, за счет полезных молочнокислых бактерий; выделяемые гнилостными микробами продукты жизнедеятельности, по мнению ученого, сокращают жизнь человека. Существуют разнообразные виды антагонизма (противодействия) микробов.
Все они связаны с конкуренцией за кислород и питательные вещества и зачастую сопровождаются изменением кислотно-щелочного баланса среды в сторону, оптимально подходящую для жизнедеятельности одного вида микроорганизмов, но неблагоприятную для его конкурента. При этом одним из наиболее универсальных и эффективных механизмов проявления микробного антагонизма является продуцирование ими разнообразных химических веществ-антибиотиков. Эти вещества способны или подавлять рост и размножение иных микроорганизмов (бактериостатическое действие), или уничтожать их (бактерицидное действие). К бактериостатическим средствам относятся такие антибиотики, как эритромицин, тетрациклины, аминогликозиды. Бактерицидные препараты вызывают гибель микроорганизмов, организму остается только справиться с выведением продуктов их жизнедеятельности. Это антибиотики пенициллинового ряда, цефалоспорины, карбапенемы и др. Некоторые антибиотики, действующие бактериостатически, уничтожают микроорганизмы, если применяются в большой концентрации (аминогликозиды, левомицетин). Но не следует увлекаться увеличением дозы, так как с повышением концентрации резко возрастает вероятность токсического влияния на клетки человека.
История открытия бактериофагов.
Бактериофаги (фаги) (от греч. phages - «пожирать») - вирусы, избирательно поражающие бактериальные клетки. Чаще всего они начинают размножаться внутри бактерий, вызывая таким образом их разрушение. Одной из областей применения бактериофагов является антибактериальная терапия, альтернативная приему антибиотиков. Например, применяются бактериофаги: стрептококковый, стафилококковый, клебсиеллезный, дизентерийный поливалентный, пиобактериофаг, коли, протейный и колипротейный и др. Бактериофаги используются также в генной инженерии в качестве векторов, переносящих участки ДНК, возможна также естественная передача генов между бактериями посредством некоторых фагов (трансдукция).
Бактериофаги были открыты независимо Ф. Твортом совместно с А. Лондом и Ф. д"Эрелем как фильтрующиеся передающиеся агенты разрушения бактериальных клеток. Первоначально полагалось, что они являются ключом к контролю над бактериальными инфекциями, однако ранние исследования оказались в основном несостоятельными. Были выделены бактериофаги, способные инфицировать большинство прокариотических групп организмов; и они легко выделяются из почвы, воды, канализационных стоков и, как и можно того ожидать, из большинства сред, колонизированных бактериями. В 1940-1950 гг. исследовательские работы по изучению структуры и физиологии взаимодействий хозяин - фаг, проведенные Г. Делбрюком, С. Луриа, А. Дерманомм, Р. Херши, И. Лвоффом и другими, заложили основание для развития молекулярной биологии, которая, в свою очередь, стала фундаментом для целого ряда новых ветвей индустрии, основанных на биотехнологии. Бактериофаги, как и другие вирусы, несут свою генетическую информацию в форме ДНК либо РНК. Большинство бактериофагов имеют хвостики, кончики которых прикреплены к конкретным рецепторам, таким как молекулы углеводов, белков и липополисахаридов на поверхности бактерии-хозяина. Бактериофаг впрыскивает свою нуклеиновую кислоту в хозяина, где он использует генетический механизм хозяина, чтобы реплицировать свой генетический материал, и считывает его, чтобы сформировать новый фагокапсульный материал для создания частичек нового фага. Число фагов, произведенных в течение единичного цикла инфекции (размер выхода), варьирует между 50 и 200 новыми фаговыми частицами. Сопротивляемость бактериофагу может развиться за счет потери или изменений в молекулах рецептора на поверхности клетки-хозяина. Бактерии также имеют особые механизмы, защищающие их от вторжения инородной ДНК. ДНК-хозяин модифицируется путем метилирования на определенных точках последовательности ДНК; это создает защиту от разложения хозяин-специфичными рестрикционными эндонуклеазами. Бактериофаги разделяются на 2 группы: вирулентные и умеренные. Вирулентные фаги вызывают литическую инфекцию, приводящую к разрушению клеток-хозяев и производящую чистые пятна (бляшки) на колониях восприимчивых бактерий. Умеренные фаги интегрируют свою ДНК посредством бактерии-хозяина, вырабатывая лизогеническую инфекцию, и геном фага передается всем дочерним клеткам при клеточном делении».
Развитие бактериофаговой терапии.
Бактериофаговая терапия (применение бактериальных вирусов для лечения бактериальных инфекций) была проблемой» весьма интересующей ученых 60 лет назад в их борьбе с бактериальными инфекциями. Открытие пенициллина и других антибиотиков в 1940-х гг. обеспечило более результативный и многосторонний подход к подавлению вирусных заболеваний и спровоцировало к закрытию работ в данной области. В Восточной Европе тем не менее исследования продолжали осуществляться и формировались некоторые способы борьбы против вирусов с использованием бактериофагов. Энтеральные и гнойно-септические заболевания, инициированные условно-патогенными возбудителями, в том числе хирургические инфекции, инфекционные заболевания детей первого года жизни, заболевания уха, горла, носа, легких и плевры; хронические клебсиеллезы верхних дыхательных путей - озена и склерома; урогенитальная патология, гастроэнтероколиты, все труднее поддаются традиционной антибактериальной терапии. Летальный исход при перечисленных инфекциях достигает 30-60%. Фактором неэффективности терапии является высокая частота устойчивости возбудителей к антибиотикам и химиотерапевтическим препаратам, достигающая 39,9-96,9%, а также подавление иммунитета как воздействие этих препаратов на организм больного, реакции токсического свойства и аллергического характера с побочными действиями, проявляющиеся в расстройствах кишечника на фоне дисбактериоза, и аналогичное расстройство верхних дыхательных путей при терапии склеромы и озены. В особенности актуальна проблема дисбактериоза кишечника у детей раннего возраста. Отдаленные результаты такого лечения у детей - иммунодепрессия, хронические септические состояния, нарушения питания, недостатки развития.
Это надо знать!
Бактериофаги - вирусы, избирательно поражающие бактериальные клетки. Чаще всего они начинают размножаться внутри бактерий, вызывая, таким образом их разрушение. Одной из областей применения бактериофагов является антибактериальная терапия, альтернатива приему антибиотиков.
Клинические исследования показали, что использование бактериофагов для обработки поверхностей помещений и отдельных объектов, например туалетов, предупреждает передачу инфекций, вызываемых Escherichia coli, у детей и взрослых. В ветеринарии доказано, что эшерихиоз у телят можно предупредить, если сбрызгивать помет в телячьих загонах водными суспензиями бактериофагов. В то время как на фазе ранних исследований был показан довольно существенный успех, фаготерапии не получилось стать общеустановленной практикой. Это было объяснено неспособностью селектировать высоковирулентные фаги, а также выбором фагов с чрезмерно узкой штамм-специфичностью. Прочие моменты содержали в себе появление фагорезистентных штаммов, нейтрализацию или вывод фагов защитными функциями иммунной системы и отслоение эндотоксинов вследствие обширного массивного бактериального разрушения клеток. Потенциальная возможность фагоопосредованной горизонтальной трансляции токсинных генов также является причиной, которая может ограничивать их использование для лечения отдельных конкретных инфекций. По предоставленным данным М. Слопеса (1983 и 1984 гг.), использование препаратов бактериофагов при инфекционных болезнях пищеварительной системы, воспалительно- гнойных изменениях кожных покровов, кровеносной системы, дыхательной системы, опорно-двигательного аппарата, мочеполовой системы (более 180 нозологических единиц заболеваний, вызванных бактериями Klebsiella, Escherichiae, Proteus, Pseudomonas, Staphylococcus, Streptococcus, Serratia, Enterobacter) показало, что препараты бакте риофагов оказывают должный эффект в 78,3-93,6% случаев и часто являются единственным эффективным лечебным средством.
В течение 2 последних десятилетий проходили некоторые экспериментальные изучения для того, чтобы подвергнуть переоценке использование терапевтических методик, основанных на использовании бактериофагов, для лечения инфекционных болезней людей и животных. Недавно результаты этих исследований были пересмотрены. Д.Смит и соратники опубликовали результаты серии опытов по лечению системных инфекций Е. Coli у грызунов и расстройства кишечника в виде диареи у телят. Доказано, что как профилактика, так и лечение, возможны, если использовать фаговые титры намного более низкие, чем число целевых организмов, что является индикацией размножения бактериофагов in vivo. Они показали, что введение внутримышечно 106 единиц E. Coli приводило к смерти 10 опытных мышей, тогда как одновременная инъекция в другую лапку 104 фагов, выбранных против К1 капсул-антигена, давала полную защиту.
Бактериофаговая терапия по соотнесению с антибиотикотерапией обладает рядом преимуществ. Например, она эффективна против лекарственно-устойчивых организмов и может использоваться в качестве альтернативной терапии пациентов, имеющих аллергии к антибиотикам. Она может использоваться профилактически с целью борьбы с распространением инфекционного заболевания там, где источник идентифицирован на ранней стадии, или там, где вспышки случаются внутри сравнительно закрытых организаций, таких как школы или дома престарелых. Бактериофаги обладают высокой специфичностью по отношению к целевым организмам и никак не влияют на организмы, не являющиеся объектами атаки. Они являются самокопирующимися и самолимитирующимися; когда организм-мишень наличествует, они самовоспроизводятся до тех пор, пока все бактерии-цели не будут заражены и уничтожены. Бактериофаги мутируют естественным образом, чтобы бороться с резистентными мутациями хозяина; кроме того, их можно подвергнуть преднамеренной мутации в лаборатории. В России и странах СНГ препараты бактериофагов применяются для лечения гнойно-септических и энтеральных заболеваний разнообразной локализации, возбужденных условно-патогенными бактериями родов Escherichia, Proteus^ Pseudomonas, Enterobacter, Staphylococcus, Streptococcus, служат заменителями антибиотиков. Они не уступают и даже превосходят последние по эффективности, не вызывая побочных токсических и аллергических л реакций и не имея противопоказаний к применению. Препараты бактериофагов эффективны при лечении болезней, вызванных антибиотикоустойчивымн штаммами микроорганизмов, в частности при лечении паратонзиллярных гнойников, воспалений пазух носа, а также гнойно-септических инфекций, реанимационных больных, хирургических заболеваний, циститов, пиелонефритов, холециститов, гастроэнтероколитов, парапроктитов, дисбактериоза кишечника, воспалительных заболеваний и сепсиса новорожденных. При обширно распространенном формировании стабильности к антибиотикам у патогенных бактерий, необходимость в новых антибиотиках и альтернативных технологиях контроля за микробными инфекциями завоевывает все большую значимость. Бактериофагам, вероятно, еще предстоит исполнить свою роль в лечении инфекционных заболеваний как при их независимом применении, так и в сочетании с антибиотико-терапией.
Изобретатель
: Александр Флеминг
Страна
: Великобритания
Время изобретения
: 3сентября 1928 г.
Антибиотики - одно из замечательнейших изобретений XX века в области медицины. Современные люди далеко не всегда отдают себе отчет в том, сколь многим они обязаны этим лечебным препаратам.
Человечество вообще очень быстро привыкает к поразительным достижениям своей науки, и порой требуется сделать некоторое усилие для того, чтобы представить себе жизнь такой, какой она была, к примеру, до изобретения , радио или .
Так же быстро вошло в нашу жизнь огромное семейство разнообразных антибиотиков, первым из которых был пенициллин.
Сегодня нам кажется удивительным, что еще в 30-х годах XX столетия ежегодно десятки тысяч людей умирали от дизентерии, что воспаление легких во многих случаях кончалось смертельным исходом, что  сепсис был настоящим бичом всех хирургических больных, которые во множестве гибли от заражения крови, что тиф считался опаснейшей и трудноизлечимой болезнью, а легочная чума неизбежно вела больного к смерти.
сепсис был настоящим бичом всех хирургических больных, которые во множестве гибли от заражения крови, что тиф считался опаснейшей и трудноизлечимой болезнью, а легочная чума неизбежно вела больного к смерти.
Все эти страшные болезни (и многие другие, прежде неизлечимые, например, туберкулез) были побеждены антибиотиками.
Еще более поразительно влияние этих препаратов на военную медицину. Трудно поверить, но в прежних войнах большинство солдат гибло не от пуль и осколков, а от гнойных заражений, вызванных ранением.
Известно, что в окружающем нас пространстве находятся мириады микроскопических организмов микробов, среди которых немало и опасных возбудителей болезней. В обычных условиях наша кожа препятствует их проникновению внутрь  организма.
организма.
Но во время ранения грязь попадала в открытые раны вместе с миллионами гнилостных бактерий (кокков). Они начинали размножаться с колоссальной быстротой, проникали глубоко внутрь тканей, и через несколько часов уже никакой хирург не мог спасти человека: рана гноилась, повышалась температура, начинался сепсис или гангрена.
Человек погибал не столько от самой раны, сколько от раневых осложнений. Медицина оказывалась бессильна перед ними. В лучшем случае врач успевал ампутировать пораженный орган и тем останавливал распространение болезни.
Чтобы бороться с раневыми осложнениями, надо было научиться парализовать микробов, вызывающих эти осложнения, научиться обезвреживать попавших в рану кокков. Но как этого достигнуть? Оказалось, что воевать с микроорганизмами можно непосредственно с их же помощью, так как одни микроорганизмы в процессе своей жизнедеятельности выделяют вещества, способные уничтожать другие микроорганизмы.
Идея использовать микробов в борьбе с микробами появилась еще в XIX веке. Так, Луи Пастер открыл, что  бациллы сибирской язвы погибают под действием некоторых других микробов. Но понятно, что разрешение этой проблемы требовало огромного труда - нелегко разобраться в жизни и взаимоотношениях микроорганизмов, еще труднее постичь, какие из них находятся во вражде друг с другом и чем один микроб побеждает другого.
бациллы сибирской язвы погибают под действием некоторых других микробов. Но понятно, что разрешение этой проблемы требовало огромного труда - нелегко разобраться в жизни и взаимоотношениях микроорганизмов, еще труднее постичь, какие из них находятся во вражде друг с другом и чем один микроб побеждает другого.
Однако сложнее всего было вообразить, что грозный враг кокков уже давно и хорошо известен человеку, что он уже тысячи лет живет бок о бок с ним, то и дело  напоминая о себе. Им оказалась обыкновенная плесень - ничтожный грибок, который в виде спор всегда присутствует в воздухе и охотно разрастается на всем старом и отсыревшем, будь то стена погреба или кусок .
напоминая о себе. Им оказалась обыкновенная плесень - ничтожный грибок, который в виде спор всегда присутствует в воздухе и охотно разрастается на всем старом и отсыревшем, будь то стена погреба или кусок .
Впрочем, о бактерицидных свойствах плесени было известно еще в XIX веке. В 60-х годах прошлого века между двумя русскими врачами - Алексеем Полотебновым и Вячеславом Манассеиным - возник спор. Полотебнов утверждал, что плесень является родоначальником всех микробов, то есть что все микробы происходят от нее. Манассеин же доказывал, что это неверно.
Чтобы обосновать свои доводы, он стал исследовать зеленые плесени (по-латыни пенициллиум глаукум). Он посеял плесень на питательной среде и с изумлением отметил: там, где рос плесневой грибок, никогда не развивались бактерии. Из этого Манассеин сделал вывод, что плесневой грибок препятствует росту микроорганизмов.
То же потом наблюдал и Полотебнов: жидкость, в которой появлялась плесень, оставалась всегда прозрачной,  стало быть, не содержала бактерий. Полотебнов понял, что как исследователь он был не прав в своих заключениях. Однако как врач он решил немедленно исследовать это необычное свойство такого легкодоступного вещества, как плесень.
стало быть, не содержала бактерий. Полотебнов понял, что как исследователь он был не прав в своих заключениях. Однако как врач он решил немедленно исследовать это необычное свойство такого легкодоступного вещества, как плесень.
Попытка увенчалась успехом: язвы, покрытые эмульсией, в которой содержался плесневой грибок, быстро заживали. Полотебнов сделал интересный опыт: он покрывал глубокие кожные язвы больных смесью плесени с бактериями и не наблюдал в них никаких осложнений, В одной из своих статей 1872 году он рекомендовал таким же образом лечить раны и глубокие нарывы. К сожалению, опыты Полотебнова не привлекли к себе внимания, хотя от послераневых осложнений во всех хирургических клиниках тогда погибало множество народа.
Вновь замечательные свойства плесени были открыты спустя полвека шотландцем Александром Флемингом. С юности Флеминг мечтал найти вещество, которое могло бы уничтожать болезнетворных бактерий, и упорно занимался микробиологией.
Лаборатория Флеминга помещалась в маленькой комнате отдела патологии одного из крупных лондонских  госпиталей. В этой комнате всегда было душно, тесно и беспорядочно. Чтобы спастись от духоты, Флеминг все время держал окно открытым. Вместе с другим врачом Флеминг занимался исследованиями стафилококков.
госпиталей. В этой комнате всегда было душно, тесно и беспорядочно. Чтобы спастись от духоты, Флеминг все время держал окно открытым. Вместе с другим врачом Флеминг занимался исследованиями стафилококков.
Но, не закончив работы, этот врач ушел из отдела. Старые чашки с посевами колоний микробов еще стояли на полках лаборатории - уборку своей комнаты Флеминг всегда считал напрасной тратой времени.
Однажды, решив писать статью о стафилококках, Флеминг заглянул в эти чашки и обнаружил, что многие из находившихся там культур покрыла плесень. Это, впрочем, было неудивительно - очевидно, споры плесени занесло в лабораторию через окно. Удивительным было другое: когда Флеминг стал исследовать культуру, то во многих  чашках не оказалось и следа стафилококков - там была только плесень и прозрачные, похожие на росу капли.
чашках не оказалось и следа стафилококков - там была только плесень и прозрачные, похожие на росу капли.
Неужели обычная плесень уничтожила всех болезнетворных микробов? Флеминг немедленно решил проверить свою догадку и поместил немного плесени в пробирку с питательным бульоном. Когда грибок развился, он поселил в ту же различные бактерии и поставил ее в термостат. Исследовав затем питательную среду, Флеминг обнаружил, что между плесенью и колониями бактерий образовались светлые и прозрачные пятна - плесень как бы стесняла микробов, не давая им расти около себя.
Тогда Флеминг решил сделать более масштабный опыт: пересадил грибок в большой сосуд и стал наблюдать за его развитием. Вскоре поверхность сосуда покрылась « » - разросшимся и сбившимся в тесноте грибком. «Войлок» несколько раз менял свой цвет: сначала он был белым, потом зеленым, потом  черным. Менял цвет и питательный бульон - из прозрачного он превратился в желтый.
черным. Менял цвет и питательный бульон - из прозрачного он превратился в желтый.
«Очевидно, плесень выделяет в окружающую среду какие-то вещества», - подумал Флеминг и решил проверить, обладают ли они вредными для бактерий свойствами. Новый опыт показал, что желтая жидкость разрушает те же микроорганизмы, которые разрушала и сама плесень. Причем жидкость обладала чрезвычайно большой активностью - Флеминг разводил ее в двадцать раз, а раствор все равно оставался губительным для болезнетворных бактерий.
Флеминг понял, что стоит на пороге важного открытия. Он забросил все дела, прекратил другие исследования. Плесневый грибок пенициллиум нотатум отныне целиком  поглотил его внимание. Для дальнейших экспериментов Флемингу понадобились галлоны плесневого бульона - он изучал, на какой день роста, при какой и на какой питательной среде действие таинственного желтого вещества окажется наиболее эффективным для уничтожения микробов.
поглотил его внимание. Для дальнейших экспериментов Флемингу понадобились галлоны плесневого бульона - он изучал, на какой день роста, при какой и на какой питательной среде действие таинственного желтого вещества окажется наиболее эффективным для уничтожения микробов.
В то же время выяснилось, что сама плесень, так же как и желтый бульон, оказались безвредными для животных. Флеминг вводил их в вену кролику, в брюшную полость белой мыши, омывал бульоном кожу и даже закапывал ее в глаза - никаких неприятных явлений не наблюдалось. В пробирке разведенное желтое вещество - продукт, выделяемый плесенью, - задерживало рост стафилококков, но не нарушало функций лейкоцитов крови. Флеминг назвал это вещество пенициллином.
С этих пор он постоянно думал над важным вопросом: как выделить действующее активное вещество из профильтрованного плесневого бульона? Увы, это оказалось чрезвычайно сложным делом. Между тем было ясно, что вводить в кровь человека неочищенный бульон, в котором содержался чужеродный белок, безусловно, опасно.
Молодые сотрудники Флеминга, такие же, как и он, врачи, а не химики, предприняли множество попыток  разрешить эту проблему. Работая в кустарных условиях, они потратили массу времени и энергии но ничего не добились. Всякий раз после предпринятой очистки пенициллин разлагался и терял целебные свойства.
разрешить эту проблему. Работая в кустарных условиях, они потратили массу времени и энергии но ничего не добились. Всякий раз после предпринятой очистки пенициллин разлагался и терял целебные свойства.
В конце концов, Флеминг понял, что эта задача ему не по плечу и что разрешение ее следует передать другим. В феврале 1929 года он сделал в Лондонском медицинском научно-исследовательском клубе сообщение о найденном им необыкновенно сильном антибактериальном средстве. Это сообщение не обратило на себя внимания.
Однако Флеминг был упрямый шотландец. Он написал большую статью с подробным изложением своих экспериментов и поместил ее в научном журнале. На всех конгрессах и медицинских съездах он так или иначе делал напоминание о своем открытие. Постепенно о  пенициллине стало известно не только в Англии, но и в Америке.
пенициллине стало известно не только в Англии, но и в Америке.
Наконец, в 1939 году два английских ученых - Говард Флори, профессор патологии одного из оксфордских институтов, и Эрнст Чейн, биохимик, бежавший из Германии от преследования нацистов, - обратили на пенициллин самое пристальное внимание.
Чейн и Флори искали тему для совместной работы. Трудность задачи выделения очищенного пенициллина привлекла их. В Оксфордском университете оказался штамм (культура микробов, выделенная из определенных источников), присланный туда Флемингом. С ним-то они и стали экспериментировать.
Для того чтобы превратить пенициллин в лекарственный препарат, его необходимо было связать с каким-нибудь веществом, растворимым в воде, но таким образом, чтобы, будучи очищенным, он не терял своих удивительных свойств. Долгое время эта задача казалась неразрешимой - пенициллин быстро разрушался в кислой среде (поэтому, кстати, его нельзя было принимать внутрь) и очень недолго сохранялся в щелочной, он легко переходил в эфир, но, если его не ставили на лед, разрушался и в нем.
 Только после многих опытов жидкость, выделенную грибком и содержащую аминопенициллиновую кислоту, удалось сложным путем отфильтровать и растворить в специальном органическом растворителе, в котором не растворялись соли калия, хорошо растворимые в воде. После воздействия ацетата калия в осадок выпали белые кристаллы калийной соли пенициллина. Проделав множество манипуляций, Чейн получил слизистую массу, которую ему удалось наконец превратить в коричневый порошок.
Только после многих опытов жидкость, выделенную грибком и содержащую аминопенициллиновую кислоту, удалось сложным путем отфильтровать и растворить в специальном органическом растворителе, в котором не растворялись соли калия, хорошо растворимые в воде. После воздействия ацетата калия в осадок выпали белые кристаллы калийной соли пенициллина. Проделав множество манипуляций, Чейн получил слизистую массу, которую ему удалось наконец превратить в коричневый порошок.
Первые же опыты с ним имели потрясающий эффект: даже маленькая гранула пенициллина, разведенная в пропорции один на миллион, обладала мощным бактерицидным свойством - помещенные в эту среду смертоносные кокки гибли через несколько минут. В то же время введенный в вену препарат не только не убил ее, но вообще не произвел на зверька никакого действия.
К опытам Чейна присоединилось еще несколько ученых. Действие пенициллина всесторонне исследовали на белых мышах. Их заражали стафилококками и стрептококками в дозах более чем смертельных. Половине из них ввели пенициллин, и все эти мыши остались живы. Остальные умерли через несколько . Вскоре было открыто, что пенициллин губит не только кокков, но и возбудителей гангрены.
 В 1942 году пенициллин опробовали на больном, который умирал от менингита. Очень скоро тот поправился. Известие об этом произвело большое впечатление. Однако наладить производство нового препарата в воюющей Англии не удалось. Флори отправился в США, и здесь в 1943 году в городе Пеории лаборатория доктора Когхилла впервые начала промышленное производство пенициллина. В 1945 году Флемингу, Флори и Чейну за их выдающиеся открытие была присуждена Нобелевская премия.
В 1942 году пенициллин опробовали на больном, который умирал от менингита. Очень скоро тот поправился. Известие об этом произвело большое впечатление. Однако наладить производство нового препарата в воюющей Англии не удалось. Флори отправился в США, и здесь в 1943 году в городе Пеории лаборатория доктора Когхилла впервые начала промышленное производство пенициллина. В 1945 году Флемингу, Флори и Чейну за их выдающиеся открытие была присуждена Нобелевская премия.
В СССР пенициллин из плесени пенициллиум крустозум (этот грибок был взят со стены одного из московских бомбоубежищ) получила в 1942 году профессор Зинаида Ермольева. Шла война. Госпитали были переполнены ранеными с гнойными поражениями, вызванными стафилококками и стрептококками, осложнявшими и без того тяжелые раны.
Лечение было трудным. Много раненых умирало от гнойного заражения. В 1944 году после долгих исследований Ермольева отправилась на фронт, чтобы испытать действие своего препарата. Всем раненым перед операцией Ермольева делала внутримышечную инъекцию пенициллина.  После этого у большинства бойцов раны рубцевались без всяких осложнений и нагноений, без повышения температуры.
После этого у большинства бойцов раны рубцевались без всяких осложнений и нагноений, без повышения температуры.
Пенициллин показался видавшим виды полевым хирургам настоящим чудом. Он вылечивал даже самых тяжелых больных, уже болевших заражением крови или воспалением легких. В том же году в СССР было налажено заводское производство пенициллина.
В дальнейшем семья антибиотиков стала быстро расширяться. Уже в 1942 году Гаузе выделил грамицидин, а в 1944 году американец украинского происхождения Ваксман получил стрептомицин. Началась эра антибиотиков, благодаря  которым в последующие годы сохранили жизнь миллионы людей.
которым в последующие годы сохранили жизнь миллионы людей.
Любопытно, что пенициллин так и остался незапатентованным. Те, кто его открыли и создали, отказались получать патенты - они считали, что вещество, которое может принести такую пользу человечеству, не должно служить источником дохода. Вероятно, это единственное открытие таких масштабов, на которое никто не предъявлял авторских прав.
Безусловно, существует просто огромное количество лекарственных препаратов, всевозможных антибиотиков, БАДов, история открытия которых не известна людям и на сегодняшний день. Но вот что нельзя оставить без внимания, так это открытие такого известного антибиотика, как пенициллин.
Первым антибиотиком, который был открыт случайно, является именно легендарный пенициллин. Бензилпенициллин (пенициллин G (PCN G) или просто пенициллин (PCN)) - N-фенилацетамид 6-аминопенициллановой кислоты. Антибиотик, получаемый из плесневого гриба пенициллиума. Необходимо отметить тот момент, что его действие основывается на процессе подавления того синтеза, который участвует в оболочках внешнего типа, а также он относится еще и к клеткам бактериальной категории - бензилпенициллин препятствуют размножению клеток прокариот, в том числе и цианобактерий, а также препятствуют делению хлоропластов.
Примерно в 1929 году хорошо известный в то время британский бактериолог Александр Флеминг проводил серию экспериментов по изучению плесневых грибов. Он установил, что определенный вид плесневых грибов выделяет специфическое антибактериальное вещество, позже названное пенициллином. Именно его опыты были посвящены подробному изучению влияния бактериальных инфекций на организм человека.
После того как в ходе экспериментов были выращены первые колонии стафилококковых культур, Флеминг выявил, что большинство из них подвержены заражению плесневым грибом Penicillium chrysogenum. Британский ученый обратил свое внимание на ту область, где стафилококковые бактерии не размножались - как раз там, где находились плесневые грибы Penicillium notanum. Таким образом, он пришел к выводу, что определенного вида плесень способна вырабатывать вещества, которые просто убивают бактерии, соприкасающиеся с ней. Результатом экспериментов стало выделение бактериологом Флемингом антимикробного препарата, названного пенициллином. Словом, это бы первейший антибиотик современного типа.
Как действует пенициллин?
Что касается принципа работы прославленного антибиотика, то он заключается в том, что происходит процесс торможения и подавления химических реакций, необходимых для того, чтобы бактерии «жили». За счет действия пенициллина осуществляется блокирование молекул, которые участвуют в зарождении и строительстве совершенно новых клеток микробов. Мало того, очень важным необходимо считать и тот момент, что пенициллин G не оказывает практически никакого негативного влияния на организм человека, либо животного. Наружные оболочки клеток человека очень сильно отличаются от аналогичных клеток, которыми обладает бактерия.

Еще в 1931 году были предприняты попытки как-то улучшить само качество лекарственного препарата, а также получить его в весьма чистой форме. Но, к сожалению, на первых порах все это не увенчалось успехом, и до серийного производства пенициллина прошло еще около десяти лет.

В начале 40х годов 20го века английским бактериологам Хоуарду У. Флори, а также биохимикам Эрнсту Чейну и Норману У. Хитли впервые удалось получить качественную чистую форму пенициллина PCN G. Что спасло жизни сотен тысяч, если не миллионов раненных солдат во время второй мировой войны! Именно за это ученым была присуждена Нобелевская премия по физиологии и медицине «за открытие пенициллина и его целебного воздействия при различных инфекционных болезнях», Флеминг, Флори и Чейн получили её в 1945 году.

Именно благодаря пенициллину, было спасено огромное количество жизней, как во время второй мировой войны, так и после. Более того, лекарство стало первейшим средством, которое способно противостоять микробам самых различных классов и видов. Открытие и производство пенициллина является одним из величайших событий в медицине и науке ушедшего века.
Конечно, на сегодняшний день разработано немыслимое количество разнообразных антибиотиков, но всегда стоит помнить, что большинство из этих препаратов основаны именно на открытии лечебных свойств пенициллина!
Как ни печально, до 20 века многие болезни были неизлечимы, а лечение других требовало недюжинных способностей как врача, так и пациента, и изрядной доли везения. Впрочем, медики, всерьёз озабоченные проблемами выживаемости своих пациентов, искали решения, которые позволили бы успешно бороться с заболеваниями.
Когда стало известно, что причиной многих заболеваний, а также послеоперационных осложнений (главным образом в военных полевых госпиталях) являются микроорганизмы - бактерии и микробы, начались поиски способов по из обезвреживанию.
Довольно быстро пришли к выводу, что бороться с болезнетворными бактериями можно с помощью других микроорганизмов, враждебным к болезнетворным. Эта идея возникла еще в 19 веке. Так, например, знаменитый французский микробиолог, Луи Пастер открыл, что бациллы сибирской язвы погибают под действием некоторых других микробов. Но на поиски наиболее действенных способов решения имеющейся задачи требовалось невероятное количество времени, терпения и труда.
Или вмешательства Его Величества Случая, без которого, кажется, не было сделано ни одно по-настоящему великое открытие. С пенициллином вышло именно так: случай и блестящая догадка.
Полезная плесень
Всё начинается с плесени. С самой обыкновенной зеленовато-серой плесени, которая берется неизвестно откуда в углах плохо проветриваемых помещений или покрывает несвежие продовольственные продукты.
Плесень - это микроскопический грибок, возникающий из еще меньших зародышей, тысячи которых носятся в воздухе. При попадании в благоприятную для роста среду, они начинают очень быстро разрастаться.
Об антибактериальном эффекте плесени, а точнее одной из её разновидностей - грибка Penicillium - было известно еще в незапамятные времена. Упоминания об использовании плесени для лечения гнойных заболеваний встречаются в трудах Авиценны (11 век) и Филиппа фон Гогенгейма, более известного под именем Парацельс (16 век).
Бактерицидные свойства плесени активно обсуждались и исследовались и в 19 веке. А в 60-ых годах позапрошлого века между двумя российскими медиками - Алексеем Полотебновым и Вячеславом Манассеиным - даже разгорелась самая настоящая научная дискуссия.
А.Полотебнов утверждал, что плесень - родоначальник всех микробов, в то время как В.Манассеин отстаивал совершенно противоположную точку зрения. Для подтверждения своих утверждений, он занялся исследованиями культур зелёной плесени.
Он посеял споры плесени в питательную среду и по результатам наблюдений отметил: там, где рос плесневой грибок, бактерии не развивались. Из этого был сделан закономерный вывод о том, что плесневой грибок препятствует росту других микроорганизмов.
Тот же процесс затем пронаблюдал и А.Полотебнов, признавший в итоге, что отстаивал неверную точку зрения. Полотебнов настолько заинтересовался результатами опытов, что занялся собственными исследованиями бактерицидных свойств плесени. Он даже применял полученные культуры плесени для лечения трудно заживающих кожных язв.
Попытка увенчалась успехом: язвы, покрытые эмульсией, в которой содержался плесневой грибок, быстро заживали. В одной из своих публикаций 1872 года А.Полотебнов рекомендовал использовать плесень для лечения кожных повреждений, однако его идея не завоевала популярность и была, можно сказать, забыта.
Александр Флеминг
Именно он "открыл" чудодейственный пенициллин повторно, спустя полвека после работ В.Манассеина и А.Полотебнова. Несколько фактов из биографии А.Флеминга.
Александр Флеминг, родился 6 августа 1881 года, шотландский бактериолог, был членом Королевского колледжа хирургов. После вступления Британии в первую мировую войну Флеминг служил капитаном в медицинском корпусе Королевской армии, участвовал в военных действиях во Франции.
Одним из первых открытий Флеминга стало заключение о том, что карболовая кислота (фенол), широко применявшаяся для обработки открытых ран, убивает лейкоциты, создающие в организме защитный барьер, что способствует в итоге выживанию бактерий в тканях.
В 1922 году после ряда неудачных попыток выделить возбудителя простудных заболеваний Флеминг открыл (чисто случайно!) лизоцим - фермент, убивающий некоторые бактерии и не причиняющий вреда здоровым тканям. Название открытого фермента было придумано профессором Райтом.
Увы, о широком применении лизоцима не могло идти и речи: перспективы медицинского использования лизоцима оказались довольно ограниченными. Впрочем, это подтолкнуло Флеминга к поиску других антибактериальных препаратов.
Так в 1928 году, благодаря очередной счастливой случайности и наблюдательности учёного, был открыт пенициллин.

Открытие пенициллина
Какой набор случайных совпадений привёл к эпохальному открытию - достоверно установить проблематично. Даже рассказы о том, как Флеминг обнаружил необычные свойства плесени в чашке Петри на своём лабораторном столе довольно противоречивы.
По одним данным Флеминг не отличался особой аккуратностью и не выбрасывал культуры по 2-3 недели, пока его лабораторный стол не оказывался загроможденным 40-50 чашками. Тогда он принимался за уборку, просматривал культуры одну за другой, чтобы не пропустить что-нибудь интересное.
По другой версии, плесень "надуло" в случайно оставленную открытой чашку Петри с культурой стафилококков из распахнутого настежь окна.
Ну а по третьей версии события развивались несколько иначе. Флеминг был очень аккуратен в обращении с культурами кокков в лабораторной посуде, так как если их оставляли не закрытыми, они моментально покрывались плесенью. На одну из таких случайно забытых чашек Флеминг и обратил своё внимание, когда обнаружил, что культура покрылась плесенью, но как-то по-особенному: между плесенью и колониями бактерий образовались светлые и прозрачные пятна - плесень как бы стесняла микробов, не давая им расти около себя. Тогда Флеминг решил сделать более масштабный опыт: пересадил грибок в большой сосуд и стал наблюдать за его развитием.
Спорить о том, как оно было на самом деле бесполезно. Тем более, сегодня открытие пенициллина - свершившийся факт.
Флеминг проникся значимостью своего открытия не сразу. Первое время он рисовал пенициллином картины . Правда, параллельно с этим он изучал свойства вещества, проводя ряд опытов на животных. Отрицательных реакций не наблюдалось, на содержании лейкоцитов в крови не менялось, а бактерицидный свойства пенициллина были очевидны.
Первым человеком, к которому был применён пенициллин, был ассистент Флеминга доктор Стюарт Греддок, заболевший гайморитом. Ему ввели в гайморову полость небольшое количество вещества, и уже через три часа состояние его здоровья значительно улучшилось.
Так 13 сентября 1929 года на заседании медицинского исследовательского клуба при Лондонском университете Александр Флеминг сообщил о своих исследованиях.
Очистка и массовое производство пенициллина
До широкого применения пенициллина в медицинне было ещё далеко: необходимо было очистить полученное вещество от посторонних примесей. Удалось этого добиться далеко не сразу: только в 1938 году группа ученых Оксфордского университета, получившая на проведение исследований грант в размере $5 тысяч от фонда Рокфеллера, сумела добиться нужного результата.

Возглавлял группу профессор Оксфорда Говард Флори, а в состав группы входили: биохимик Эрнст Чейн, конструктор Норман Хитли, который с успехом использовал новейшие для того времени технологии лиофилизации (выпаривание посредством низких температур), а также Александр Флеминг - душа проекта. За своё открытие учёные в 1945 году получили Нобелевскую премию
Шла Вторая мировая война и наладить массовое производство лекарства в Англии не было никакой возможности. Осенью 1941 года Флори и Хитли отправились в Америку, где предложили технологию производства пенициллина председателю научно-исследовательского медицинского совета США Альфреду Ричардсу. Согласие на финансирование программы было получено на высочайшем уровне.
Американцам удалось разработать эффективную технологию глубинного брожения. Первый завод стоимостью в 200 млн долларов был построен менее чем за год, причем батареи его огромных ферментеров, где выращивалась плесень, напоминали оборудование для обогащения урана.
Вслед за этим в США и Канаде были построены новые заводы. Производство пенициллина росло как на дрожжах: июнь 1943 года - 0,4 млрд. единиц, сентябрь - 1,8 млрд., декабрь - 9,2 млрд., март 1944 года - 40 млрд. единиц. Уже в марте 1945 года пенициллин появился в американских аптеках.
После окончания войны вышел скандал: Америка всерьёз настраивалась присвоить идею и технологию производства себе, но с помощью нескольких публикаций в прессе англичане убедительно доказали всему миру свой приоритет в изобретении пенициллина.

Пенициллин в России
В годы Великой Отечественной Иосиф Сталин добивался увеличения поставок в СССР американского пенициллина. При этом он настаивал на том, что производство этого лекарства должно быть освоено и в СССР. Даже велись переговоры с американцами о покупке лицензии на производство пенициллина.
Представители США озвучили астрономическую сумму, да ещё и дважды её повышали, аргументируя это "ошибкой в предварительных расчётах". В итоге микробиолог Зинаида Ермольева занялась производством отечественного аналога, получившего название крустозин . По своим свойствам это вещество значительно уступало пенициллину, да и технология его производства была невероятно дорогой.
Кончилось всё это тем, что лицензия на производство пенициллина была куплена у Эрнста Чейна, после чего НИИ эпидемиологии и гигиены Красной Армии, под руководством Николая Копылова, освоил эту технологию и запустил ее в производство.
Основным производственным штаммом была культура Penicillium chrysogenum. В 1945 году после испытаний отечественного пенициллина коллектив института во главе с Копыловым был удостоен Сталинской премии. Ермольева же и её крустазин были преданы забвению.
Несмотря на все замечательные свойства антибиотиков вообще и пенициллина в частности, сегодня учёные озабочены тем, насколько быстро большинство бактерий и микробов вырабатывает устойчивость к их воздействию.
Так директором Европейского регионального бюро Всемирной организации здравоохранения был сделан неутешительный вывод: "Ещё Александр Флеминг предостерегал, что чрезмерное увлечение антибиотиками формирует у бактерий сопротивляемость к этим медикаментам. Если все будет идти так же, как и сейчас, то вскоре наступит время, когда против некоторых бактерий просто не будет лекарств".
Наша редакция желает читателям крепкого здоровья и напоминает, что препараты, являющиеся антибиотиками, отпускаются из аптек только по рецепту врача . Будьте здоровы!
Penicillium chrysogenium (notatum) — один из представителей рода Penicillium. «Рекордсмен» по выработке пенициллина
Сама идея применять для борьбы с микроорганизмами другие микроорганизмы (или то, что они синтезируют), витала в медицине очень давно.
В самом микробном сообществе одни микробы постоянно подавляют другие и находятся в таком динамическом равновесии.
Еще в 1897 году, задолго до открытия пенициллина, Эрнест Дюшен использовал в эксперименте плесень для лечения тифа у морских свинок.

Penicillium roqueforti — «благородная плесень». Используется для приготовления сыра рокфор и дает ему своеобразный вкус
Как думаете, что общего у морских свинок, сыра с плесенью и водопроводной воды?
Вопрос довольно сложный. Казалось бы: ничего общего. Но если бы вы были французским студентом-медиком конца 19 века, то эти предметы были бы вашими научными реагентами.
Эти реагенты использовал блестящий Эрнест Дюшен для обнаружения антибиотиков, практически за 35 лет до того, когда Александр Флеминг открыл пенициллин.
Так что история антибитиков началась не с Флеминга, нет. Флеминг не был первым, кто заметил антибактериальные свойства плесени. Плесень применяли для лечения ран древние египтяне. И, хотя в Древнем Египте не было научной опоры многим медицинским действиям, не стоит забывать о замечательной наблюдательности древних врачевателей.
Эрнест Дюшен
 Именно он первый описал антибактериальные свойства пенициллина. О его жизни известно совсем немного. Он родился в Париже, обучался в военной медицинской школе в Лионе, куда поступил в двадцатилетнем возрасте.
Именно он первый описал антибактериальные свойства пенициллина. О его жизни известно совсем немного. Он родился в Париже, обучался в военной медицинской школе в Лионе, куда поступил в двадцатилетнем возрасте.
Дюшен был просто очарован микробами. Еще бы! Открытие болезнетворных свойств у микробов, труды Луи Пастера, просто перевернули мировоззрение медиков того времени. Эрнест Дюшен решил написать диссертацию под руководством профессора микробиологии Габриэля Ру. Габриэль Ру тогда руководил лабораторией, которая отвечала за качество водоснабжения в Лионе. Диссертационная работа Дюшена была посвящена следующему наблюдению: водопроводная вода никогда не заплесневала, но плесень могла хорошо расти в дистилированной воде. Первым возникло предположение, что бактерии не дают плесени расти в водопроводной воде.
Эрнест выращивал Penicillum glaucum. Эта плесень применяется для изготовления сыров горгондзола и стилтон. Он помещал ее в емкости с водопроводной и кипяченой водой. Потом он добавил возбудителя брюшного тифа и кишечную палочку — плесень быстро умерла. Выяснилось, что бактерии в воде убивают плесень. Дюшен начал задавать разные условия: температура, кислотность среды, но плесень погибала не всегда. Иногда победа оставалась за грибком.
Опять возник вопрос: а плесень может чем то «ответить» бактерии? Может ли она с ними бороться? В эксперименте на морских свинках было обнаружено снижение вирулентности бактерий. Более того, путем инъекции плесени Дюшен смог вылечить животное. Подобный эксперимент проведет Александр Флеминг, которого нередко и называют открывателем пенициллина.
О том, как был открыт пенициллин Флемингом, написано очень много. Так почему же Дюшенна не помнят как открывателя пенициллина? На это есть несколько причин. Ну, во-первых он исследовал Penicillum glausum, в отличие от другого вида плесени Penicillum notanum. Плесень, которая фактически этот пенициллин и синтезирует. Уже позднее было установлено, что Penicillum glausum продуцирует другой, более слабый антибиотик — патулин (кстати, токсичен и работает в высоких концентрациях, поэтому не применяется). Вероятно, если бы не здоровье молодого ученого, а также недолгий жизненный путь (умер от туберкулеза в 1912 году, потеряв задолго до этого от того же туберкулеза свою жену), открытие пенициллина принадлекжало бы ему.
Александр Флеминг
 Но факт есть факт. Автором и первооткрывателем пенициллина был Александр Флеминг. Датой открытия самого известного антибиотика является 3 сентября 1928 года (День рождения пенициллина). Флеминг к тому времени был уже широко известен, имел репутацию блестящего исследователя.
Но факт есть факт. Автором и первооткрывателем пенициллина был Александр Флеминг. Датой открытия самого известного антибиотика является 3 сентября 1928 года (День рождения пенициллина). Флеминг к тому времени был уже широко известен, имел репутацию блестящего исследователя.
Открытию пенициллина человечество обязано все же этому шотландскому биохимику. После Первой мировой войны, в которой «отец пенициллина» служил военным врачом, Флеминг не мог смириться с тем, что большое количество солдат погибали от инфекционных осложнений. В 1918 году он вернулся с войны работать в бактериологическую лабораторию больницы Св. Марии, где он работал до этого (и где проработает до самой смерти). В 1922 году произошел случай, больше конечно похожий на басню, но тем не менее на шесть лет опередивший открытие пенициллина. Простуженный Флеминг случайно чихнул на чашку Петри, где находились бактериальные колонии. Через несколько дней он обнаружил замедленный рост бактерий (Micrococcus lysodeikticus) на некоторых местах. Так был открыт лизоцим (мурамидаза). Это гидролитический фермент расщепляет стенки бактерий, то есть обладающий бактерицидными свойствами. Много его в выделениях носовой слизи, слюне (почему животные могут зализывать раны), слезной жидкости. Много его и в грудном молоке (причем заметно больше, чем в коровьем и при кормлении со временем концентрация его не уменьшается, а возрастает). Конечно, когда будет открыт пенициллин, интерес к лизоциму заметно упадет, вплоть до открытия лизоцима куриного белка.
Как отмечал в последующем сам Александр Флеминг, открытию пенициллина помог случай. Работая в лаборатории и изучая фермент лизоцим, Флеминг не отличался порядком на рабочем месте (хотя порядок у ученых свой!). Как это нередко бывает с гениями (вспомнить хотя бы рабочий стол Эйнштейна), в лаборатории ученого был сущий бардак. Флеминг, вернувшись после месяца отсутствия заметил, что на одной чашке с культурами стафилококка появились плесневые грибы. Колония грибка растворила высеянную культуру . Плесень принадлежала к роду пеницилловых, поэтому выделенное вещество потом и назвали пенициллином.

Название пенициллина переводится как «кисточка для письма», подобная схожесть видна под микроскопом
Говард Флори
 И хотя, когда речь заходит об открытии пенициллина, вспоминают Александра Флеминга, практическую пользу из этого открытия извлекли другие ученые, в частности фармаколог Говрад Уолтер Флори. В 1938 году Флори, работая совместно с Эрнестом Чейном и Норманом Хитли в Оксфортском университете, в Англии, начали проводить эксперименты с антибактериальными свойствами грибка Penicillium notatum. О свойствах грибка подавлять бактериальный рост писал в своих трудах Флеминг.
И хотя, когда речь заходит об открытии пенициллина, вспоминают Александра Флеминга, практическую пользу из этого открытия извлекли другие ученые, в частности фармаколог Говрад Уолтер Флори. В 1938 году Флори, работая совместно с Эрнестом Чейном и Норманом Хитли в Оксфортском университете, в Англии, начали проводить эксперименты с антибактериальными свойствами грибка Penicillium notatum. О свойствах грибка подавлять бактериальный рост писал в своих трудах Флеминг.
Первым пациентом, которому был назначен пенициллин, был Альберт Александр, лондонский полицейский. Серезная инфекция, затронувшая часть лица, периорбитальной области глаза, волосистой части головы, началась с небольшого укола шипом розы. Флори и Чейн дали больному пенициллин и в течение первых суток намечалась хорошая динамика. Однако, определить оптимальную дозу лекарства не удалось (ее еще тогда и не знали) и инфекционный процесс все же привел к смерти пациента. Эксперименты продолжились, препарат назначали серьезно больным детям с впечатляющим эффектом. Сейчас считают, что труды Флори и Чейна спасли более 80 миллионов человек.
Эрнест Чейн
 А теперь стоит сказать, об упоминавшемся ранее, биохимике Эрнесте Борисе Чейне. Родившийся в еврейской семье и проживая в Германии, был вынужден с приходом к власти Гитлера эмигрировать в Англию. Как сополучатель в будущем Нобелевской премии за открытие пенициллина, Чейн был за ту часть работы, в которой он показал строение пенициллина и успешно выделил активное вещество. Чтобы выделить пенициллин, для одной терапевтической дозы, было необходимо переработать около 500 литров питательного бульона с плесенью!
А теперь стоит сказать, об упоминавшемся ранее, биохимике Эрнесте Борисе Чейне. Родившийся в еврейской семье и проживая в Германии, был вынужден с приходом к власти Гитлера эмигрировать в Англию. Как сополучатель в будущем Нобелевской премии за открытие пенициллина, Чейн был за ту часть работы, в которой он показал строение пенициллина и успешно выделил активное вещество. Чтобы выделить пенициллин, для одной терапевтической дозы, было необходимо переработать около 500 литров питательного бульона с плесенью!
Чейн писал: «Трудности, с которыми столкнулся Флеминг, только подстегнули мой интерес к обнаруженному Флемингом пенициллину. Я сказал Флори, что мы найдем способ хотя бы частично очистить пенициллин, несмотря на его нестойкость».
В 1938 году Чейн и его коллега Норман Хитли быстро пришли к выводу, что пенициллин, в отличие от лизоцима — это не фермент, а небольшая молекула органического происхождения.
Небольшие размеры молекулы обнадежили исследователей: будет легко расшифровать молекулярную структуру и синтезировать его. О том, что будет легко, ученые ошибались…
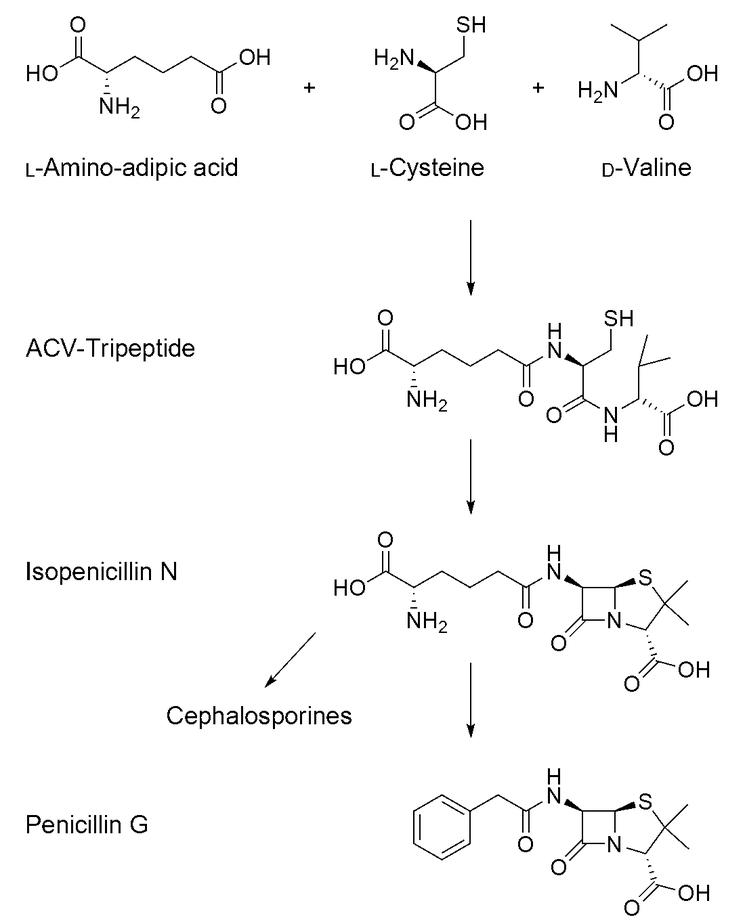
Было установлено, что в состав пенициллина входит комплекс структур, которые в последующем назвали бета-лактамами.
О возможности существования подобной структуры Чейн предполагал и ранее, но вопрос решился только в 1949-м.
 Когда при помощи рентгенологической кристаллографии Дороти Ходжкин определила расположение атомов в кристаллической решетке пенициллина. Именно после 1949 года, после определения точной молекулярной структуры пенициллина, стало возможным массовое дешевеое производство препарата.
Когда при помощи рентгенологической кристаллографии Дороти Ходжкин определила расположение атомов в кристаллической решетке пенициллина. Именно после 1949 года, после определения точной молекулярной структуры пенициллина, стало возможным массовое дешевеое производство препарата.
Кстати, Дороти Ходжкин тоже получила Нобелевскую премию за исследование кристаллической решетки в рентгеновских лучах, в 1964 году. Эта выдающаяся женщина заложила основы метода, с помощью которого стало возможным исследование структуры ДНК (программа «Геном человека»).
Чейн и Флори для получения пенициллина в концентрированном виде, применили новую тогда методику лиофилизации. Раствор пенициллина замораживался, а затем при низкой температуре и низком давлении вода изгонялась, оставляя ценный материал.
Penicillium chrysogenium (notatum): как нашли самый «пенициллиновый» грибок
С начала Второй мировой войны резко возросла потребность в пенициллине. Необходимость в таком лекарстве была очевидна.
В 1940 году группа ученых Оксфордского университета (которую и возглавляли Флори и Чейн) достала из запасников пенициллин Флеминга и начала искать способы его производства в большом количестве.
Так как начались бомбежки Лондона и возник риск оккупации, ученые отправились на переговоры в Нью-Йорк (вероятность высадки немцев была так велика, что Чейн даже пропитал свой пиджак целебной плесенью, объяснив коллегам: в случае чего спасать в первую очередь этот пиджак).
В нью-Йорке приехавших ученых встретили без особого энтузиазма: выработка пенициллина редко превышала 4 единицы действия на 1 миллилитр питательной среды. Это очень мало: на флаконе с пенициллином, к примеру, написано «1 000 000 ЕД». Для одной дозы препарата нужно было переработать 250 литров бульона.
Сразу обрисовалась цель: найти самый «урожайный» грибок. Сначала ученые отправились в Пеорию (штат Иллинойс), где находилась исследовательская лаборатория по изучению метаболизма плесени. Сотрудники лаборатории собрали значительную коллекцию, но лишь немногие штаммы плесени могли производить пенициллин.
Начали подключать знакомых: чтобы присылали образцы почвы, плесневых зерен, фруктов и овощей. Наняли одну женщину, чтобы она обходила магазины, пекарни, сыроварни, отыскивая новые образцы сине-зеленой плесени. Ее звали мисс Мэри Хант, за хорошую работу прозванная «Плесневелая Мэри».
Ход истории изменила дыня кантатула, на которой поселился сине-зеленый грибок. Эта плесень производила 250 единиц пенициллина на миллилитр питательной среды. Один из мутировавших из нее штаммов стал производить 50000 единиц! Все штаммы, продуцирующие пенициллин на сегодня — это потомки той самой плесени, которую нашли в 1943 году. Это был грибок Penicillium chrysogenium, ранее называвшийся Penicillium notatum.
С того момента и началась эпоха промышленного производства пенициллина.
Когда в 1945 году Флемингу, Флори и Чейну вручали Нобелевскую премию по физиологии и медицине, Флеминг сказал: «Говорят, что это я изобрел пенициллин. Но человек не мог его изобрести — это вещество создано природой. Я не изобретал пенициллин, я всего лишь обратил на него внимание людей и дал ему название» .

Флеминг, Чейн и Флори на вручении Нобелевской премии
Если вы нашли опечатку в тексте, пожалуйста, сообщите мне об этом. Выделите фрагмент текста и нажмите Ctrl+Enter .






